Nước H2O là trong những chất rất rất gần gũi và nhập vai trò đặc biệt trong đời sống thực tế, nước tham gia vào nhiều quá trình hóa học đặc trưng của nhỏ người cũng tương tự động thực trang bị khác.
Bạn đang xem: Tính chất hóa học của nước hóa 8
Vậy nước H2O gồm thành phần kết cấu như cố nào, tính chất hóa học và đặc thù vật lý ra sao? có vai trò gì cùng được ứng dụng vào nghành nghề dịch vụ nào trong đời sống sản xuất, bọn họ cùng khám phá qua nội dung bài viết dưới đây.
I. Thành phần cấu tạo của NƯỚC H2O
- Nước là hợp hóa học được tạo bởi 2 yếu tố là Hidro cùng Oxi (H cùng O) chúng đã hóa hợp với nhau với tỉ trọng thể tích là một phần khí O2 với 2 phần khí H2 (tỉ lệ khối lượng là 1 phần Hidro cùng 8 phần Oxi) có công thức phân tử là H2O.
1. Sự phân hủy nước
- lúc cho cái điện một chiều đi qua Nước, trên mặt phẳng 2 điện rất sẽ hình thành Hidro cùng Oxi.
2H2O -điện phân→ 2H2 + O2
2. Sự tổng thích hợp nước
- Đốt các thành phần hỗn hợp H2 và O2 bởi tia lửa điện gây nổ và 1 thể tích khí Oxi sẽ hóa phù hợp với 2 thể tích khí Hidro để tạo thành thành nước.
2H2 + O2
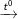
II. đặc điểm vật lý của Nước H2O
- Nước là chất lỏng không màu, không mùi, không vị, sôi sinh sống 100°C (ở áp suất khí quyển là 760 milimet Hg), hóa rắn sinh sống 0°C thành nước đá với tuyết.
- Khối lượng riêng biệt của nước sinh hoạt 4°C là 1 g/ml (hoặc 1 kg/lít).
- Nước rất có thể hòa tan được rất nhiều chất rắn (đường, muối bột ăn,...) chất lỏng (axit, cồn,..) và hóa học khí (Hidroclorua HCl, Amoniac NH3,...)
III. Tính chất hóa học của Nước H2O
1. Nước công dụng với Kim loại
- Nước công dụng được với một trong những kim nhiều loại ở ánh sáng thường như: Li, Na, K, Ca,... Sản xuất thành bazơ với khí H2.
• H2O + Kim loại → Bazơ + H2↑
2Na + 2H2O → 2NaOH + H2 ↑
2K + 2H2O → 2KOH + H2 ↑
Ca + 2H2O → Ca(OH)2 + H2 ↑
2. Nước chức năng với Oxit bazo
- Nước tác dụng với Oxit bazo chế tác thành bazơ tương ứng, dung dịch bazơ làm quỳ tím chuyển màu xanh.
• H2O + Oxit → Bazơ
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2
3. Nước chức năng với Oxit axit
- Nước tính năng với Oxit axit tạo thành Axit tương ứng, dung dịch axit làm quỳ tím thay đổi màu sắc đỏ.
• H2O + Oxit axit → Axit
SO2 + H2O → H2SO3
SO3 + H2O → H2SO4
P2O5 + 3H2O → 2H3PO4
IV. Phương châm và áp dụng của Nước
- Nước hoà tan nhiều chất dinh dưỡng quan trọng cho khung người sống
- Nước tham gia với nhiều quá trình hoá học quan trọng trong khung người người và đụng vật.
- Nước rất cần thiết cho cuộc sống hàng ngày, sản suet nông nghiệp, công nghiệp, xây dung, giao thông vận tải vận tải.
* giữ ý: để giữ lại nguồn nước ko bị ô nhiễm cần
- ko thải rác rưởi xuống sông, hồ, kênh, ao..
- xử lý nước thải sinh hoạt với nước thải công nghiệp trước khi cho tung vào hồ, sông.
V. Bài tập về Nước
Bài 1 trang 125 sgk hóa 8: Dùng từ, nhiều từ
- Nước là hợp hóa học tạo vì hai ... Là ... Và ... Nước công dụng với một trong những ... ở ánh sáng thường và một trong những ... Tạo nên bazơ; tính năng với những ... Tạo thành axit.
* lời giải bài 1 trang 125 sgk hóa 8:
- Nước là hợp chất tạo do hai nguyên tố là oxi và hiđro. Nước công dụng với một số kim loại ở ánh sáng thường với một số oxit bazơ tạo bắt buộc bazơ; chức năng với oxit axittạo ra axit.
Xem thêm: Địa Chỉ Bán Bánh Mì Doner Kebab Ngon Ở Hà Nội, Kebab Ngon Nhất Tại Hà Nội
Bài 2 trang 125 sgk hóa 8: Bằng những cách thức nào có thể chứng tỏ được nhân tố định tính và định lượng của nước? Viết những phương trình chất hóa học xảy ra?
* giải mã bài 2 trang 125 sgk hóa 8:
- Bằng phương pháp phân hủy nước bởi dòng năng lượng điện hoặc tổng hợp nước (thực nghiệm) để chứng tỏ thành phần định tính và định lượng của nước, phương trình chất hóa học như sau:
2H2O - điện phân→ 2H2↑ + O2↑
2H2 + O2
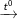
Bài 3 trang 125 sgk hóa 8: Tính thể tích khí hiđro cùng oxi(đktc) cần công dụng với nhau để tạo nên được 1,8g nước.
* giải mã bài 3 trang 125 sgk hóa 8:
- Theo bài xích ra, cần tạo thành 1,8g nước, bắt buộc ta có:
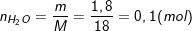
- Phương trình phản ứng:
2H2 + O2 → 2H2O.
- Theo PTPƯ, thì ta có:
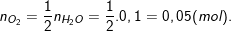
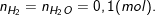
⇒ Thể tích Oxi ở ĐKTC là: VO2 = n.22,4 = 0,05.22,4 = 1,12(lít).
⇒ Thể tích Hidro nghỉ ngơi ĐKTC là: VH2 = n.22,4 = 0,01.22,4 = 2,24(lít).
Bài 4 trang 125 sgk hóa 8:Tính cân nặng nước sinh hoạt trạng thái lỏng vẫn thu được khí đốt cháy hoàn toàn 112l khí hiđro (đktc) với oxi?
* Lời giải bài 4 trang 125 sgk hóa 8:
- Theo bài bác ra, đốt cháy 112 lít khí khí Hidro, yêu cầu có:
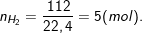
- Phương trình hóa học phản ứng tổng hợp nước:
2H2 + O2 → 2H2O.
- Theo PTPƯ: nH2O = nH2 = 5 (mol).
⇒ mH2O= n.M = 5.18 = 90(g).
⇒ Vì trọng lượng riêng của nước là 1g/ml phải thể tích nước lỏng thu được là 90ml.
Bài 5 trang 125 sgk hóa 8: Viết phương trình những phản ứng chất hóa học tao ra bazơ cùng axit. Làm nạm nào để nhận thấy được dung dịch axit cùng dung dịch bazơ?
* giải thuật bài 5 trang 125 sgk hóa 8:
- Phương trình hóa học các phản ứng tạo nên bazơ và axit:
2Na + 2H2O → 2NaOH + H2↑
Na2O + H2O → 2NaOH.
SO3 + H2O → H2SO4.
P2O5 + 3H2O → 2H3PO4.
* nhận biết dung dịch axit:
- có tác dụng quỳ tím chuyển màu đỏ.
- tác dụng với kim loại, muối bột cacbonat tất cả khí bay lên.
* phân biệt dung dịch bazơ:
- Quỳ tím gửi màu xanh.
- Phenolphtalein ko màu đưa sang màu hồng.
Hy vọng với nội dung bài viết chi huyết về tính hóa học hóa học, phương pháp phân tử của nước sống trên giúp ích cho các em. Các góp ý và thắc mắc các em vui vẻ để lại phản hồi dưới nội dung bài viết để dhn.edu.vn ghi nhận và hỗ trợ, chúc các em học tập tốt.