Kim loại bao gồm những đặc điểm vật lý cùng hóa học gì và lại được ứng dụng rất nhiều trong thực tiễn từ phần lớn vật nhỏ tuổi như mẫu kim xuất xắc lớn như máy bay, tàu ngầm,...
Bạn đang xem: Giải bài tập tính chất hóa học của kim loại
Chúng ta hãy cùng mày mò những tính chất hóa học của Kim loại trong bài viết này. Qua đó giúp những em nắm rõ những loài kiến thức căn nguyên thật giỏi để ôn với thi bậc trung học phổ thông sau này.
* đặc thù hóa học của kim loại:
Tác dụng với OxiTác dụng cùng với phi kim khácTác dụng cùng với AxitTác dụng cùng với MuốiChi tiết những phương trình làm phản ứng, lấy một ví dụ và bài xích tập họ cùng tìm hiểu dưới đây;

I. đặc điểm hóa học tập của kim loại
1. Chức năng với oxi
- sắt kẽm kim loại (trừ Au, Ag, Pt) chức năng với oxi chế tạo oxit kim loại.
PTPƯ: kim loại + O2 → Oxit kim loại
2Mg + O2 → 2MgO
2Al + 3O2 → 2Al2O3
3Fe + 2O2 → Fe3O4
2. Tính năng với phi kim khác
+ Tác dụng với Cl2: tạo thành muối clorua (kim loại bao gồm hóa trị cao nhất)
PTPƯ: Kim một số loại + Cl2 → Muối
Cu + Cl2 → CuCl2
2Al + 3Cl2 → 2AlCl3
2Fe + 3Cl2 → 2FeCl3
- Nếu fe dư: Fedư + FeCl3 → FeCl2
+ Tác dụng với giữ huỳnh: lúc đun nóng tạo ra muối sunfua (trừ Hg xảy ra ở ánh nắng mặt trời thường)
Cu + S
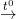
Fe + S
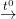
Hg + S → HgS
- lưu giữ ý: Thủy ngân tương đối độc, tránh việc tiếp xúc thẳng với thủy ngân.
3. Chức năng với Axit
+ với dụng dịch axit HCl, H2SO4 loãng
PTPƯ: Kim các loại + Axit(dd loãng) → Muối + H2↑
Fe + HCl → FeCl2 + H2↑
Zn + H2SO4 loãng → ZnSO4 + H2↑
+ Với axit H2SO4 đặc
2Ag + H2SO4 đặc, nóng→ Ag2SO4 + SO2↑ + 2H2O
2Al + 6H2SO4 đặc, lạnh → Al2(SO4)3 + 3SO2↑ + 6H2O
4. Tác dụng với dung dịch muối
- sắt kẽm kim loại mạnh đẩy sắt kẽm kim loại yếu hơn thoát ra khỏi muối, tạo ra thành muối bắt đầu và kim loại mới.
PTPƯ: Kim một số loại + Muối → Muối(mới) + Kim loại↓(mới)
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Nhận xét: Cu hoạt động hóa học mạnh mẽ hơn Ag
Fe + CuSO4 → FeSO4 + Cu
Nhận xét: Fe chuyển động hóa học to gan lớn mật hơn Cu
Dãy điện hoá kim loại:
K > mãng cầu > Ca > Mg > Al > Zn > fe > Ni > Sn > Pb > H > Cu > Hg > Ag > Pt > Au
Cách nhớ: khi nào Cần thiết lập Áo Záp Sắt nhìn Sang buộc phải Hỏi siêu thị Á Pi Âu
II. Bài tập về đặc điểm hóa học của Kim loại
Bài tập 4 trang 51 sgk hóa 9: phụ thuộc vào tính hóa chất của kim loại, hãy viết các phương trình chất hóa học biểu diễn các chuyển hóa sau đây:
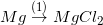
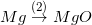
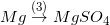
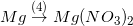
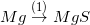
* Lời giải bài tập 4 trang 51 sgk hóa 9:
- các phương trình bội nghịch ứng:
1) Mg + Cl2 → MgCl2
2) 2Mg + O2 → 2MgO
3) Mg + H2SO4,loãng → MgSO4 + H2↑
4) Mg + 2AgNO3 → Mg(NO3)2 + 2Ag↓
5) Mg + S → MgS
Bài tập 6 trang 51 sgk hóa 9: ngâm một lá kẽm vào 20g hỗn hợp muối đồng sunfat 10% cho tới khi bội nghịch ứng kết thúc. Tính cân nặng kẽm sẽ phản ứng với hỗn hợp trên cùng nồng độ xác suất của hỗn hợp sau bội nghịch ứng.
* lời giải bài tập 6 trang 51 sgk hóa 9:
- Ta có: C% = (mct / mdd). 100%
⇒ mCuSO4 = (C%.mdd)/100 = (20.10)/100 = 2 (g).
nCuSO4 = m/M = 2/160 = 0,0125 (mol)
Zn + CuSO4 → ZnSO4 + Cu↓
1mol 1 mol 1mol 1 mol
? 0,0125 mol ?
- Theo PTPƯ ta có: nZn = nCuSO4 = 0,0125 (mol).
⇒ mZn = 0,0125. 65 = 0,8125 (g).
nZnSO4 = 0,0125 (mol)
⇒ mZnSO4 = 0,0125. 161 = 2,0125 (g)
- Theo PTPƯ nCu = nCuSO4 = 0,0125 (mol) ⇒ mCu= 64. 0,0125 = 0,8 (g).
⇒ mdd sau phản ứng = mZn + mCuSO4 - mCu = 0,8125 + đôi mươi – 0,8 = 20,0125 (g)
⇒ C%ZnSO4 = (mct / mdd). 100% = (2,0125/20,0125). 100% = 10,056%
⇒ Kết luận: mZn = 0,8125 (g); C%ZnSO4 = 10,056%
Bài tập 7 trang 51 sgk hóa 9: Ngâm một lá đồng trong 20 ml dung dịch bội nghĩa nitrat tính đến khi đồng thiết yếu tan thêm được nữa. đem lá đồng ra, cọ nhẹ, có tác dụng khô và cân nặng thì thấy trọng lượng lá đồng tăng lên 1,52 g. Hãy xác định nổng độ mol của dung dịch bạc bẽo nitrat đã dùng (giả thiết tổng thể lượng bội bạc giải phóng dính hết vào lá đồng).
* giải thuật bài tập 7 trang 51 sgk hóa 9:
- Ta gồm PTPƯ:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
- Theo PTPƯ: Thì 1 mol Cu phản ứng vừa đủ với AgNO3 sẽ tạo 2 mol Ag
⇒ Khối lượng tương ứng (do bội bạc bám vào, đồng tan ra) tăng là: 108.2 - 64 = 152g.
- Theo bài, cân nặng tăng 1,52g ⇒ nCu pư = 1,52/152 = 0,01 (mol).
- Theo PTPƯ nAgNO3 = 2.nCu = 2. 0,01 = 0,02 mol
⇒ Nồng độ hỗn hợp AgNO3: cm AgNO3 = n/V = 0,02/0,02 = 1(M).
Bài tập 6 trang 58 sgk hóa 9: Để xác minh phần trăm cân nặng của hỗn hợp A tất cả nhôm cùng magie, người ta thực hiện hai thử nghiệm sau:
– thử nghiệm 1: mang lại m gam hỗn hợp A tác dụng với dung dịch H2SO4 loãng dư, chiếm được 1568ml khí ở đk tiêu chuẩn.
– nghiên cứu 2: đến m gam hỗn hợp A chức năng với hỗn hợp NaOH dư thì sau phản ứng thấy còn lại 0,6g chất rắn.
Tính phần trăm trọng lượng của mỗi chất trong hỗn hợp A.
* Lời giải bài bác tập 6 trang 58 sgk hóa 9:
- Ở thí nghiệm 2: vì NaOH dư đề xuất Al sẽ tính năng hết với NaOH, còn Mg ko phản ứng nên cân nặng chất rắn còn lại là Mg, mMg = 0,6g.
⇒ nMg = 0,6/24 = 0,025 mol
Ta call số mol của Al là x(tức nAl = x); PTPƯ
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑ ( 1)
Mg + H2SO4 → MgSO4 + H2↑ (2)
- Theo PTPƯ (2) nH2 = nMg = 0,025 mol
- Theo PTPƯ (1) nH2 = (3/2). NAl = (3/2). X mol
⇒ toàn bô mol H2 là nH2 = 0,025 + 3x/2 mol (∗)
- Theo đề bài bác ta có: VH2 = 1568ml = 1,568 (l).
⇒ nH2 = 1,568/22,4 = 0,07 mol (∗∗)
- trường đoản cú (∗) cùng (∗∗) ⇒ 0,025 + 3x/2 = 0,07
- Giải ra ta có : x = 0,03 mol ⇒ mAl = 0,03 x 27 = 0,81g
⇒ mhỗn phù hợp A = 0,81 + 0,6 = 1,41 g
⇒ % mAl = (0,81 x 100%)/1,41 = 57,45%
⇒ % mMg = 100% - 57,45% = 42,55%.
Xem thêm: Cùng Xem Ngay Bản Đồ Tp Cần Thơ Mới Nhất, Bản Đồ Thành Phố Cần Thơ Năm 2021
Bài tập 5 trang 60 sgk hóa 9: Ngâm bột fe dư vào 10ml dung dịch đồng sunfat 1M. Sau thời điểm phản ứng kết thúc, thanh lọc được chất rắn A cùng dung dịch B.
a) Cho A tác dụng với hỗn hợp HCl dư. Tính trọng lượng chất rắn sót lại sau phản nghịch ứng.
b) Tính thể tích dung dịch NaOH 1M toàn vẹn để kết tủa trọn vẹn dung dịch B.
* giải thuật bài tập 5 trang 60 sgk hóa 9:
a) Ta bao gồm PTPƯ: sắt + CuSO4 → FeSO4 + Cu (1)
Do fe dư, nên chất rắn A tất cả sắt dư cùng đồng, hỗn hợp B là FeSO4.
- Theo bài bác ra: nCuSO4 = CM .V = 1. 0,01 = 0,01 (mol)
- Theo PTPƯ: nCu = nCuSO4 = 0,01 mol
- khi cho A tác dụng với dung dịch HCl chỉ bao gồm Fe bội nghịch ứng (Cu ko phản ứng) nên ta bao gồm PTPƯ sau:
Fe + 2HCl → FeCl2 + H2↑ (2)
- trọng lượng chất rắn sót lại sau bội nghịch ứng cùng với HCl chỉ tất cả Cu
⇒ mCu = 0,01 x 64 = 0,64g.
b) dung dịch B chỉ bao gồm FeSO4:
FeSO4 + 2NaOH → Fe(OH)2↓ + Na2SO4 (3)
Theo PTPƯ (1) thì nFeSO4 = nCuSO4 = 0,01 mol
Theo PTPƯ (3) thì nNaOH = 2.nFeSO4 = 2.0,01 = 0,02 mol
⇒ VNaOH = n/CM = 0,02/1 = 0,02 lít.
Bài 6 trang 69 sgk hóa 9: dìm một lá fe có khối lượng 2,5 gam vào 25 ml dung dịch CuSO4 15% có trọng lượng riêng là 1,12 g/ml. Sau một thời hạn phản ứng, tín đồ ta mang lá sắt thoát khỏi dung dịch, cọ nhẹ, làm cho khô thì khối lượng 2,58 gam.
a) Hãy viết phương trình hoá học.
b) Tính nồng độ phần trăm của những chất trong hỗn hợp sau làm phản ứng.
* giải thuật bài 6 trang 69 sgk hóa 9:
a) Phương trình hoá học:
Fe + CuSO4 → FeSO4 + Cu↓
1 mol 1 mol 1 mol 1 mol
b) Theo PTPƯ cứ 1 mol fe phản ứng sinh sản thành 1 mol Cu thì khối lượng thanh Fe tăng thêm là : 64 – 56 = 8 (g)
- gọi số mol fe tham gia bội phản ứng là x
- Theo bài ra số gam tăng lên sau khi lấy lá thép ra là: 2,58 – 2,5 = 0,08 (g)
⇒ x = (0,08.1)/8 = 0,01 (mol).
⇒ nFeSO4 = 0,01 mol ⇒ mFeSO4 = 0,01.152 = 1,52 (g).
⇒ mdd CuSO4 = D . V = 1,12.25 = 28 (g).
⇒ mCuSO4 = mdd.C% = 28.(15/100) = 4,2 (g)
⇒ nCuSO4 = 4,2/160 = 0,02625 (mol)
⇒ CuSO4 dư và nCuSO4 dư = 0,02625 – 0,01 = 0,01625 (mol)
- chất sau phản nghịch ứng là: FeSO4 và CuSO4 dư
⇒ mCuSO4 dư = 0,01625.160 = 2,6 (g).
⇒ mdd sau pư = 28 +2,5 – 2,58 = 27,92 (g).
⇒ C% FeSO4 = (1,52/27,92). 100 = 5,4441 (%)
⇒ C% CuSO4 dư = (2,6/27,92). 100 = 9,3123 (%)
Bài tập 7 trang 69 sgk hóa 9: Cho 0,83g lếu hợp tất cả nhôm và sắt chức năng với dung dịch H2SO4 loãng dư. Sau bội nghịch ứng thu được 0,56 lít khí nghỉ ngơi đktc.
a) Viết những phương trình hóa học.
b) Tính thành phần xác suất theo khối lượng của mỗi kim loại trong các thành phần hỗn hợp ban đầu.
* giải thuật bài tập 7 trang 69 sgk hóa 9:
a) PTPƯ:
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑ (1)
Fe + H2SO4 → FeSO4 + H2↑ (2)
b) Khí nhận được là Hyđro, theo bài bác ra ta có:
nH2 = 0,56 /22,4 = 0,025 mol.
Gọi số mol của Al cùng Fe theo thứ tự là x cùng y
Theo PTPƯ (1) thì nH2 = (3/2). NAl = (3/2). X mol
Theo PTPƯ (2) nH2 = nFe = y mol
Như vậy ta có: nH2 =
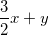
Theo bài ra, ta có: mhh = 27x + 56y = 0,83. (**)
Giải hệ phương trình (*) với (**) ta được: x =0,01; y= 0,01
⇒ mAl = 0,01 x 27 = 0,27g
⇒ mFe = 0,01 x 56 = 0,56g
Vậy %mAl = 0,27/0,83 x 100% = 32,53% ⇒ %mFe = 67,47%
Bài tập 1: mang lại 5,60 gam Fe tính năng với hỗn hợp HCl đầy đủ thu được dung dịch X. Cho dung dịch X công dụng với hỗn hợp AgNO3 thì nhận được m gam kết tủa. Biết các phản ứng là hoàn toàn, cực hiếm của m là
* khuyên bảo giải: Ta tất cả PTPƯ
Fe+ 2HCl → FeCl2 + H2↑
FeCl2 + 3AgNO3 → 2AgCl + Ag↓ + Fe(NO3)3
Theo bài xích có: nFe = m/M =5,6/56=0,1 (mol)
Theo PTPƯ ⇒ nAg = nFe = 0,1 mol; nAgCl = 2nFe = 2.0,1=0,2 (mol)
⇒ m↓ = mAg + mAgCl = 0,1.108 + 0,2.143,5 = 39,5 (g)
Bài tập 2: đến 8 gam các thành phần hỗn hợp X gồm Mg với Cu công dụng với hỗn hợp H2SO4 loãng dư. Đến khi chấm dứt phản ứng nhận được 4,48 lít khí H (đktc). Phần trăm cân nặng của Mg vào X là:
* chỉ dẫn giải: Chỉ có Mg bội phản ứng cùng với H2SO4 (loãng)
Mg+ H2SO4 → MgSO4 + H2↑
Theo PTPƯ ta có: nMg = nH2 = 4,48/22,4=0,2 (mol)
⇒ mMg = 0,2.24=4,8
⇒ %Mg = (4,8/8).100%=60%
Hy vọng cùng với phần ôn tập về tính chất hóa học của kim loại, kim loại kiềm, kiềm thổ với các ví dụ và bài xích tập vận dụng nghỉ ngơi trên hữu ích với các bạn. Những thắc mắc chúng ta hãy để lại bình luận dưới bài viết để được hỗ trợ, chúc các bạn học tập tốt.