Bài tập về cách nhận biết, tách bóc chất đội Halogen hay, cụ thể
A. Cách thức & Ví dụ
Lý thuyết và phương thức giải
Dựa vào các tính chất đặc trưng của chúng
Bạn đang xem: cách nhận thấy các chất hóa học lớp 10
a/ dìm biết một số trong những anion ( ion âm)
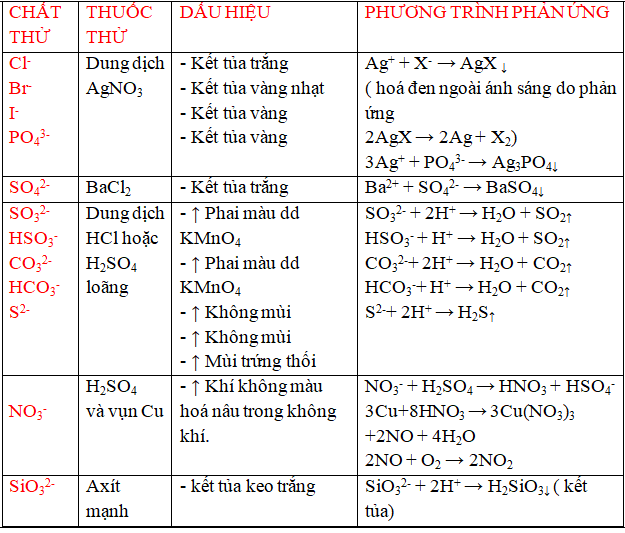
b/ nhấn biết một số trong những chất khí .
Bạn đang xem: Cách nhận biết các chất hóa học
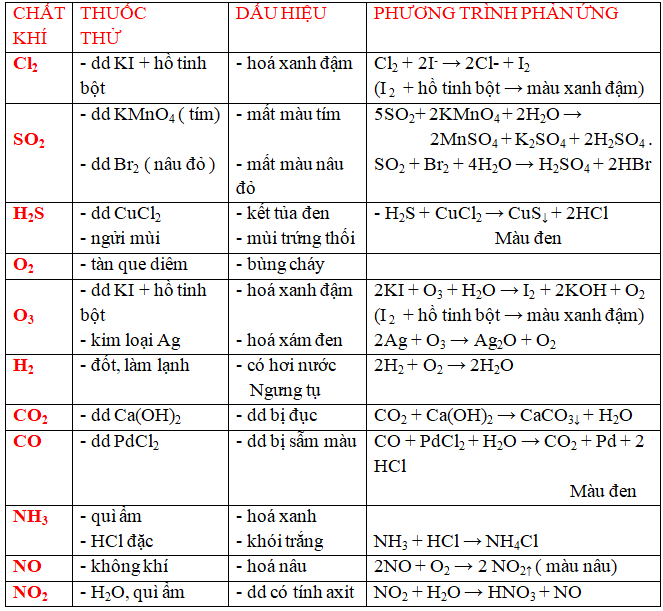
c/ thừa nhận biết một số chất khí .
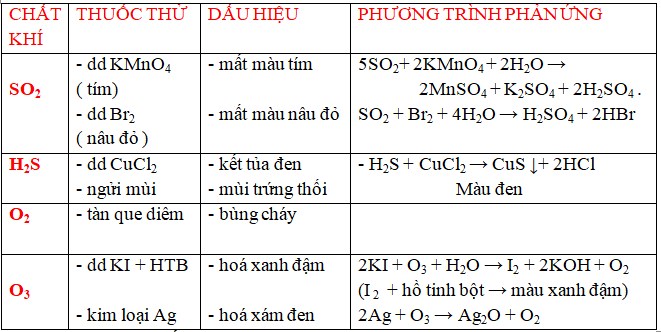
*Với bài bác tập bóc tách chất
a) bóc tách một chất thoát khỏi hỗn thích hợp :
Dạng toán này chỉ cần tách riêng một chất ra khỏi hỗn hợp, vứt bỏ các hóa học khác, ta có một trong hai biện pháp giai sau :
– biện pháp 1: cần sử dụng hóa chất phản ứng chức năng lên các chất cần loại bỏ, còn chất cần tách bóc riêng không tác dụng sau phản ứng được tách ra dễ dàng.
– bí quyết 2: dùng hóa chất tính năng với chất đề nghị muốn tách riêng tạo ra phẩm mới. Sản phẩm dễ bóc khỏi các thành phần hỗn hợp và dễ dàng tái sản xuất lại chất đầu.
b) bóc tách riêng những chất ra khỏi nhau :
Dạng toán này tách bóc riêng các chất ra khỏi nhau không được vứt chất nào. Để giải ta thực hiện đồng thời giải pháp 1, bí quyết 2 ngơi nghỉ trên nhằm giải.
Ví dụ minh họa
Ví dụ 1. Chỉ sử dụng một hóa chất, trình bày phương pháp nhận biết những dung dịch sau: KI, Zn(NO3 ) 2 , Na2 CO3 , AgNO3 , BaCl2
Hướng dẫn:
Trích mỗi dung dịch một không nhiều làm mẫu mã thử:
Cho hỗn hợp HCl lần lượt vào các mẫu thử trên.
– mẫu thử tạo hiện tượng lạ sùi bong bóng khí là Na2CO3
2HCl + Na2 CO3 → 2NaCl + CO2 + H2 O
– chủng loại thử tọa kết tủa trắng là AgNO3
AgNO3 + HCl → AgCl↓+ HNO3
Cho dung dịch AgNO3 lần lượt vào hai mẫu mã thử còn lại
– mẫu thử làm sao kết tủa trắng là dung dịch BaCl2
2AgNO3 + BaCl2 → 2AgCl↓ + Ba(NO3 ) 2
– mẫu thử sinh sản kết tủa đá quý là hỗn hợp KI
AgNO2 + KI → AgI ↓ (vàng) + KNO3
– mẫu thử không tồn tại hiện tượng gì là hỗn hợp Zn(NO3 ) 2
Ví dụ 2. Bằng phương pháp hóa học, hãy phân biệt những ung dịch đựng trong những lọ mất nhãn như sau: NaF, NaCl, NaBr, và NaI.
Hướng dẫn:
Trích mỗi dung dịch một ít làm mẫu thử:
Cho dung dịch AgNO3 thứu tự vào các mẫu demo trên.Mẫu thử làm sao trong trong cả là NaF. Bởi vì AgF chảy tốt.
– chủng loại thử chế tạo ra kết tủa trắng là NaCl
AgNO3 + NaCl → AgCl↓ + NaNO3
– chủng loại thử sinh sản kết tủa đá quý nhạt là NaBr
AgNO3 + NaBr → AgBr↓ + NaNO3
– mẫu mã thử tọa kết tủa vàng đậm là NaI
AgNO3 + NaI → AgI↓ + NaNO3
Ví dụ 3: . Bằng phương pháp hóa học. Hãy phân biệt các hỗn hợp đựng trong các lọ mất nhãn: NaCl, NaBr, NaI, HCl, H2 SO4 , KOH
Hướng dẫn:
Trích mỗi dung dịch một ít làm chủng loại thử:
Cho quỳ tím theo lần lượt vào những mẫu thử. Ta tạo thành 3 nhóm hóa chất sau:
Nhóm I: Dung dịch làm cho quỳ tím hóa xanh: KOH
Nhóm II: Dung dịch làm quỳ tím hóa đỏ: HCl, H2 SO4 .
Nhóm III: hỗn hợp không chuyển màu sắc quỳ tím: NaI, NaCl, NaBr
Cho hỗn hợp AgNO3 thứu tự vào những mẫu demo ở team (III)
– mẫu mã thử sản xuất kết tủa trắng là NaCl
AgNO3 + NaCl → AgCl↓ + NaNO3
– chủng loại thử sản xuất kết tủa quà nhạt là NaBr
AgNO3 + NaBr → AgBr↓+ NaNO3
– mẫu thử tọa kết tủa rubi đậm là NaI
AgNO3 + NaI → AgI↓+ NaNO3
Cho hỗn hợp AgNO3 thứu tự vào những mẫu test ở đội (II)
– chủng loại thử làm sao kết tủa white là HCl
AgNO3 + HCl → AgCl↓ + HNO3
– còn sót lại là H2 SO4
Ví dụ 4: Không cần sử dụng thuốc thử làm sao khác, hãy phân biệt các dung dịch: MgCl2 , NaOH, NH4 Cl, BaCl2 , H2 SO4
Hướng dẫn:
Ghi số trang bị tự 1, 2, 3, 4, 5, bên trên 5 lọ dung dịch bắt buộc nhận biết. Rót dung dịch ở mỗi lọ vào lần lượt các ống nghiệm đã làm được đánh thuộc số. Bé dại 1 dung dịch vào mẫu thử của 4 dung dịch còn lại. Sau các lần thí nghiệm cho đến khi hoàn chỉnh ta được tác dụng sau đây:
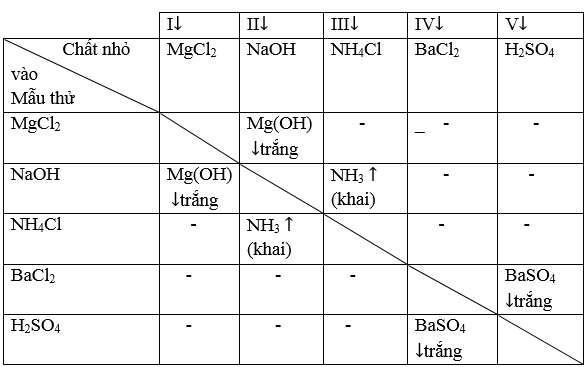
Từ bảng công dụng nhận thấy:
– hóa học nào chức năng với 4 hóa học kia sinh sản thành 1↓ + 1↑ là NaOH
– hóa học nào tạo thành khí với NaOH là NH4 Cl; chất tọa thành kết tủa cùng với NaOH và MgCl2
– Chất tác dụng với 4 hóa học khí tạo ra thành 1↓ nhưng mà khác MgCl2 là BaCl2 và chất tạo thành kết tủa cùng với BaCl2 là H2 SO4
Ví dụ 5. Brom gồm lẫn một ít tạp chất là clo. Làm ráng nào để thu được brom tinh khiết . Viết phương trình hóa học.
Hướng dẫn:
Tham khảo: kỹ năng Không khí là gì? đông đảo thành phần bầu không khí | bán Máy Nước Nóng
Cho một ít NaBr vào lếu láo hợp:
Cl2 + 2NaBr → 2NaCl + Br2
Chưng đựng hỗn hợp để đưa Br
Ví dụ 6. tinh luyện N2 trong các thành phần hỗn hợp khí N2 , CO2 , H2 S
Hướng dẫn:
Cho tất cả hổn hợp khí sục qua dung dịch nước vôi trong tất cả dư, chỉ bao gồm khí N2 không tính năng đi thoát khỏi dung dịch, hai khí còn lại phản ứng cùng với nước vôi theo phương trình bội nghịch ứng:
CO2 + Ca(OH)2 → CaCO3 ↓ + H2 O
H2 S + Ca(OH) 2 → CaS ↓ + 2H2 O
B. Bài bác tập trắc nghiệm
Câu 1. có 4 hóa học bột white color là vôi bột, bột gạo, bột thạch cao (CaSO4.2H2O) bột đá vôi (CaCO3). Chỉ dùng chất như thế nào dưới đây là nhận biết tức thì được bột gạo ?
A. Hỗn hợp HCl. B. Dung dịch H2SO4 loãng.
C. Dung dịch Br2. D. Hỗn hợp I2.
Câu 2. Để minh bạch 4 hỗn hợp KCl, HCl, KNO3, HNO3 ta hoàn toàn có thể dùng
A. Hỗn hợp AgNO3. B. Quỳ tím.
C. Quỳ tím cùng dung dịch AgNO3. D. Đá vôi.
Câu 3.
Xem thêm: Cập Nhật Dự Báo Thời Tiết Ở Phú Quốc Trong 7 Ngày Tới, Đến Du Lịch Phú Quốc Thời Gian Nào
rất có thể phân biệt 3 bình khí HCl, Cl2, H2 bằng thuốc demoA. Hỗn hợp AgNO3. B. Quỳ tím ẩm.
C. Hỗn hợp phenolphtalein. D. Không rành mạch được.
Câu 4. Chỉ cần sử dụng hóa hóa học nào sau đây để nhận ra các dung dịch: BaCl2, Zn(NO3)2, Na2CO3, AgNO3, HBr.
A. HCl B. AgNO3 C. Br2 D. Không nhận thấy được
Câu 5. Brom bao gồm lẫn một không nhiều tạp chất là clo. Một trong các hoá chất rất có thể loại bỏ clo thoát ra khỏi hỗn đúng theo là :
A. KBr. B. KCl. C. H2O. D. NaOH.
Câu 6. Dùng thuốc thử thích hợp để phân biệt các hỗn hợp sau đây: KI, HCl, NaCl, H2SO4
Câu 7. Có bố bình không ghi nhãn, từng bình đựng một trong số dung dịch NaCl, NaBr với NaI. Chỉ dùng hai thuốc thử (không cần sử dụng AgNO3), làm thay nào để xác minh dung dịch chứa trong mỗi bình ? Viết phương trình hóa học.
Câu 8. nhận ra các khí sau bằng cách thức hóa học: Cl2, O2, HCl cùng SO2
Câu 9. tinh chế NaCl bao gồm lẫn NaBr, NaI, Na2CO3.
Câu 10. Muối ăn bị lẫn tạp hóa học là Na2SO4, MgCl2, CaCl2 với CaSO4. Hãy trình bày phương thức hóa học tập để sa thải các tạp chất, thu được NaCl tinh khiết. Viết phương trình hóa học của những phản ứng.
Dạng 1: Bài tập về đặc thù hóa học và cách thức điều chế Halogen
Dạng 3: Hoàn thành phương trình chất hóa học về Halogen
Dạng 4: Kim loại tính năng với Halogen
Dạng 5: Halogen công dụng với muối bột của halogen yếu đuối hơn
Dạng 6: Muối halogen công dụng với AgNO3
Dạng 7: Bài tập về team Halogen
Giới thiệu kênh Youtube VietJack